Em 10 de março 2022 o site das Nações Unidas no Brasil, anunciou a aprovação pela Anvisa de um novo produto em terapia avançada: o Kymriah® (tisagenlecleucel), da empresa Novartis Biociências S.A.
“A aprovação dessa nova terapia genética pela ANVISA para tratar uma doença grave é mais um resultado concreto da parceria do PNUD com a agência, demonstrando a inovação que a cooperação técnica internacional pode prover. A partir da criação da RENETA, estamos apoiando o Brasil a viabilizar tratamentos avançados a todos e todas, assegurando a melhora da saúde da população, para que possa viver uma vida plena e saudável”, destaca o coordenador da Unidade de Desenvolvimento Socioeconômico Inclusivo do PNUD no Brasil, Cristiano Prado.
“Profissionais da Anvisa, com o apoio da Rede Nacional de Especialistas em Terapia Avançada (RENETA), criada mediante cooperação com o Programa das Nações Unidas para o Desenvolvimento (PNUD), empenharam-se em estabelecer avaliações técnicas e regulatórias de riscos e benefícios.”
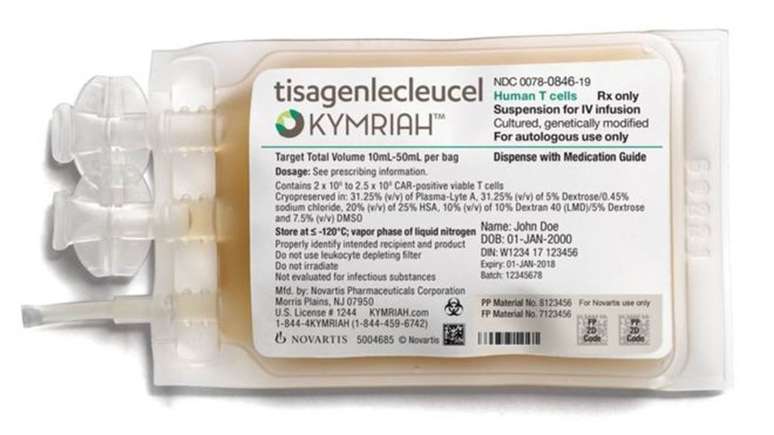
Figura 1: Tisagenlecleucel sob nome comercial Kymriah. Novartis / BBC News Brasil.
A leucemia é um tipo de câncer hematológico, que se inicia nas células-tronco existentes na medula óssea, de onde se originam as células sanguíneas. A Leucemia Linfoblástica Aguda (LLA) é um tipo de câncer comum na infância, mas também pode acometer adultos. No Brasil segundo o Instituto Nacional do Câncer (INCA), as leucemias correspondem a 26% de todas as neoplasias em crianças e adolescentes de 0 a 19 anos de idade. Dentre os sintomas é possível citar: aumento dos gânglios linfáticos, hematomas, febre, dor óssea, sangramento da gengiva, suor noturno, falta de ar e infecções frequentes.
Nesta doença, ocorre a proliferação maligna de células progenitoras linfoides na medula óssea caracterizada por um excesso de linfoblastos malignos (aproximadamente 80%) com origem nas células B.O Kymriah® (CTL019) é indicado para o tratamento de pacientes pediátricos e jovens até 25 anos de idade que apresentam Leucemia Linfoblástica Aguda (LLA) de células B, refratária ou a partir da segunda recidiva. O tratamento está igualmente indicado para pacientes adultos com Linfoma Difuso de Grandes Células B (LDGCB) recidivado ou refratário, após duas ou mais linhas de terapia sistêmica. O produto tem como alvo as células que expressam CD19, uma glicoproteína de transmembrana presente nas células B desde o desenvolvimento inicial até sua diferenciação em células plasmáticas, mas não está presente nas células-tronco sanguíneas pluripotentes e na maioria dos tecidos normais diferentes das células B. O cluster de diferenciação 19 (CD19) é expresso de modo uniforme em leucemias linfoblásticas agudas pediátricas com origem em células B. A ANVISA concluiu, por meio de análise documental, que o processo de fabricação do Kymriah® demonstra ter qualidade consistente e controlada.
O produto fora aprovado por outras autoridades regulatórias, como a Food and Drug Administration (FDA), nos Estados Unidos; a European Medicines Agency (EMA), na Europa; e a Pharmaceuticals and Medical Devices Agency (PMDA), no Japão. O país caminha para o avanço da tecnologia, sendo as Terapias Avançadas o inicio uma nova era para o tratamento do câncer. Os produtos de imunoterapia necessitam passar por diversas etapas e serem certificados como seguros até a sua aprovação.
O benefício da prolongação do tempo de vida de pacientes, por vezes, em cuidados paliativos (ou seja, sem alternativa de tratamento), se mostra soberano aos possíveis efeitos adversos. O Brasil segundo o Instituto Nacional do Câncer (INCA), as leucemias correspondem a 26% de todas as neoplasias em crianças e adolescentes de 0 a 19 anos de idade. Dentre os sintomas é possível citar: aumento dos gânglios linfáticos, hematomas, febre, dor óssea, sangramento da gengiva, suor noturno, falta de ar e infecções frequentes. Nesta doença, ocorre a proliferação maligna de células progenitoras linfoides na medula óssea caracterizada por um excesso de linfoblastos malignos (aproximadamente 80%) com origem nas células B.
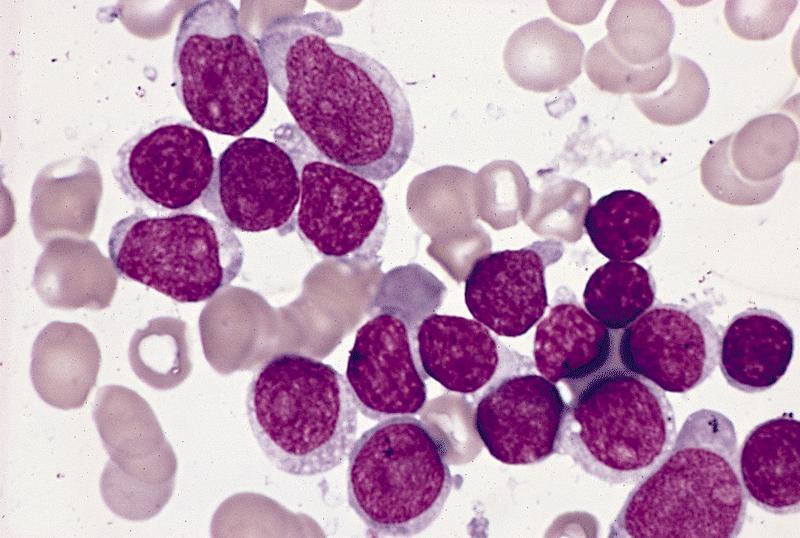
Figura 2: Linfoblastos (célula linfóide imatura com nucléolos visíveis e cromatina menos condensada) Fonte: BioSanas, Serviço de Saúde.
O Kymriah® (CTL019) é indicado para o tratamento de pacientes pediátricos e jovens até 25 anos de idade que apresentam Leucemia Linfoblástica Aguda (LLA) de células B, refratária ou a partir da segunda recidiva. O tratamento está igualmente indicado para pacientes adultos com Linfoma Difuso de Grandes Células B (LDGCB) recidivado ou refratário, após duas ou mais linhas de terapia sistêmica.
O produto tem como alvo as células que expressam CD19, uma glicoproteína de transmembrana presente nas células B desde o desenvolvimento inicial até sua diferenciação em células plasmáticas, mas não está presente nas células-tronco sanguíneas pluripotentes e na maioria dos tecidos normais diferentes das células B.
O cluster de diferenciação 19 (CD19) é expresso de modo uniforme em leucemias linfoblásticas agudas pediátricas com origem em células B. A ANVISA concluiu, por meio de análise documental, que o processo de fabricação do Kymriah® demonstra ter qualidade consistente e controlada. O produto fora aprovado por outras autoridades regulatórias, como a Food and Drug Administration (FDA), nos Estados Unidos; a European Medicines Agency (EMA), na Europa; e a Pharmaceuticals and Medical Devices Agency (PMDA), no Japão.
O país caminha para o avanço da tecnologia, sendo as Terapias Avançadas o ínicio uma nova era para o tratamento do câncer. Os produtos de imunoterapia necessitam passar por diversas etapas e serem certificados como seguros até a sua aprovação. O benefício da prolongação do tempo de vida de pacientes, por vezes, em cuidados paliativos (ou seja, sem alternativa de tratamento), se mostra soberano aos possíveis efeitos adversos.
Referências
- Confira a notícia na íntegra: https://brasil.un.org/pt-br/174481-anvisa-aprova-produto-de-terapia-avan%C3%A7ada-para-tratamento-de-c%C3%A2ncer
- Carta de Aprovação– Anvisa: https://portal.novartis.com.br/medicamentos/kymriah/
- https://www.biosanas.com.br/index.php?id=especialidade-info-item/13/leucemia-linfoide-aguda-lla
