A terapia celular é um campo da medicina regenerativa que utiliza a transferência de células humanas para substituir ou restaurar células e/ou tecidos danificados para tratar doenças e restaurar funções vitais. Essa estratégia pode empregar células obtidas do próprio paciente (terapia autóloga) ou de um doador (terapia alogênica), e podem incluir várias fontes, como células-tronco, células do sistema imunológico dentre outras células especializadas.
 Figura 1: Ilustração DNA. Gerada no canva.com
Figura 1: Ilustração DNA. Gerada no canva.com
Esta terapia tem o potencial de tratar uma ampla gama de doenças e condições, incluindo lesões musculoesqueléticas, doenças autoimunes e cânceres. As células utilizadas na terapia são manipuladas em laboratório ou em centros especializados, onde são modificadas geneticamente para que adquiram funções específicas a fim de se tornarem capazes de combater e eliminar as células disfuncionais da doença em questão.

Figura 2: Imagem iluistrativa. Obtida no freepik.
“O transplante de medula óssea é o tipo de terapia celular mais antigo já descrito. No Brasil, em 1979, um grupo pioneiro de hematologistas da Universidade Federal do Paraná deu início aos transplantes de medula óssea. Em 1983 se deu inicio no Instituto Nacional do Câncer (INCA), no Rio de Janeiro, outra unidade de transplante.” – Ferreira, Dulley, Morsoletto, Neto e Pasquini, 1985.
Alguns exemplos de terapia celular incluem:
- Terapia com células do sistema imunológico: São as células responsáveis pela defesa do corpo contra patógenos e fatores que ameacem o equilíbrio (homeostase), dentre os seus componentes podemos citar os linfócitos, granulócitos, monócitos, macrófagos, células NK, sistema complemento dentre outros. Os linfócitos podem ser divididos em duas grandes categorias: Linfócitos T (originados no timo) e Linfócitos B (originados na medula óssea). Entre eles, os linfócitos T, têm ganhado destaque nas terapias modernas e empregadas na terapia celular. Um exemplo de aplicação é a sua modificação em laboratório, onde são direcionadas a atacar células cancerígenas ou células infectadas por vírus, sendo usadas no tratamento do câncer e de algumas infecções virais.
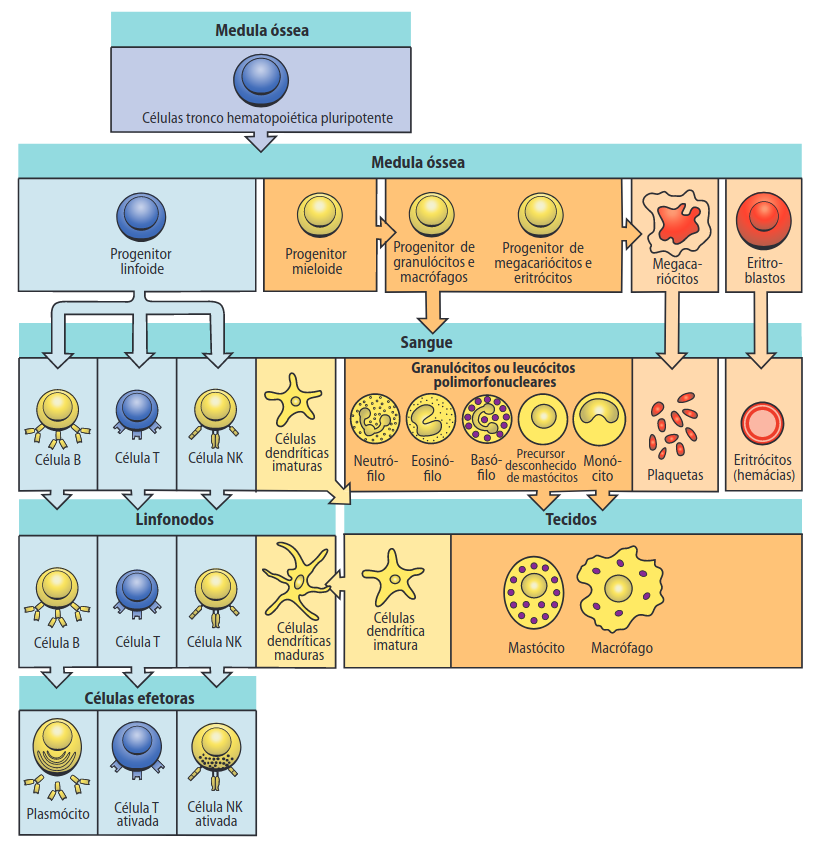
Figura 3: Adaptado de MURPHY et al., 2008, p.4
-
Terapia com células-tronco hematopoéticas (CTHs)
A terapia com CTHs (TCTH) é um tratamento que usa células-tronco do sangue e da medula óssea para restaurar o sistema sanguíneo e imunológico do paciente. Ela é indicada em doenças como leucemias, linfomas, anemias graves e imunodeficiências, nas quais a produção normal de células do sangue está comprometida.
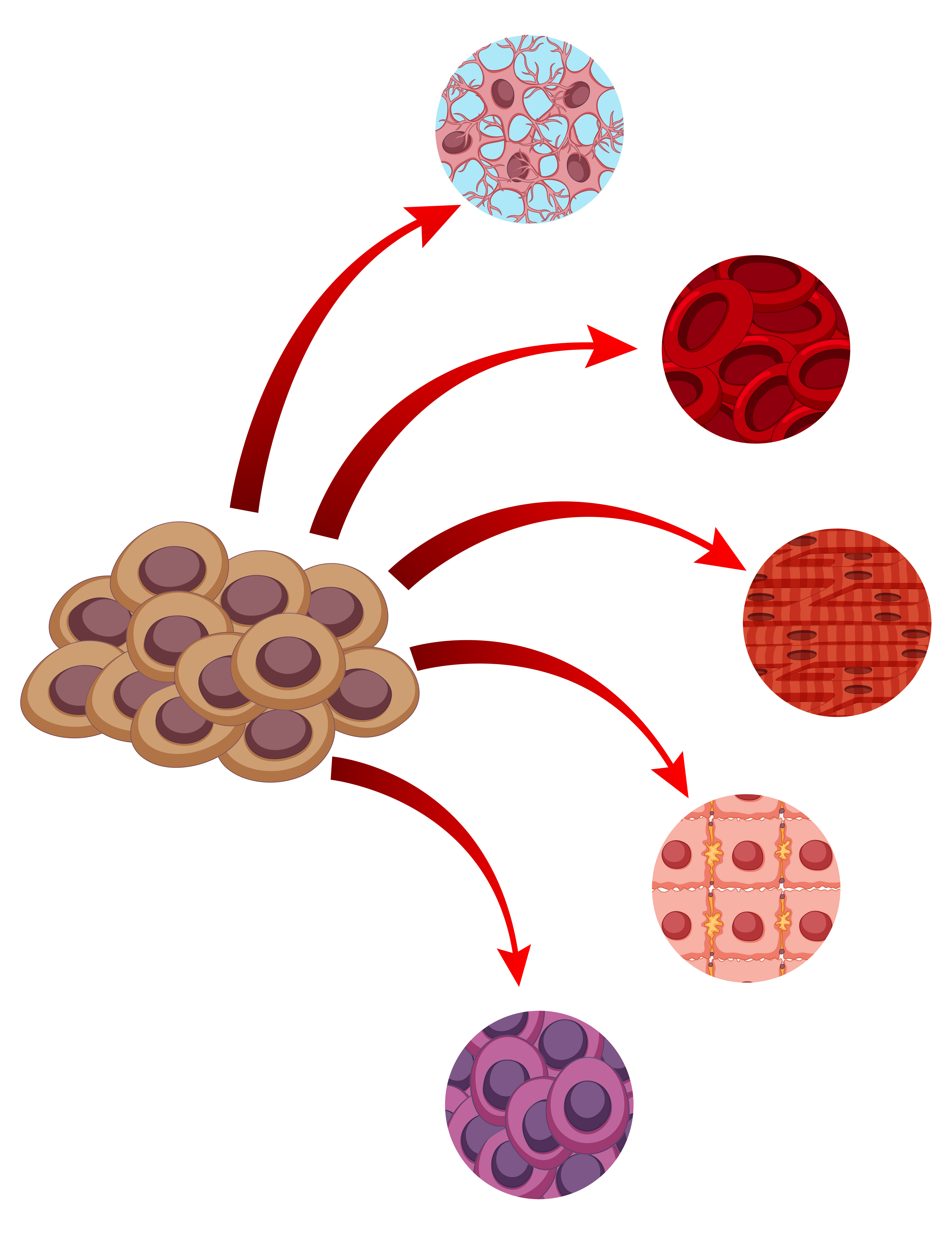 Figura 4: Célula tronco, e tipos celulares que elas são capazes de se direnciar (neurônios, célula sanguíneas, células musculares, células epiteliais, células do fígado) (Imagem obtida via brgfx no Freepik).
Figura 4: Célula tronco, e tipos celulares que elas são capazes de se direnciar (neurônios, célula sanguíneas, células musculares, células epiteliais, células do fígado) (Imagem obtida via brgfx no Freepik).
Como uma área em ascensão nos últimos anos, pesquisadores têm conseguido expandir em laboratório (ex vivo) as células-tronco obtidas do sangue do cordão umbilical, o que aumenta as chances de sucesso nos transplantes. Além disso, a terapia gênica tem sido usada para corrigir mutações genéticas diretamente nas células-tronco, abrindo assim um caminho para tratamentos personalizados. Outros estudos, exploram o uso dessas células na terapêutica de doenças autoimunes, como lúpus e esclerose múltipla.
As CTHs possuem diversas funções, entre elas a produção contínua das células sanguíneas — como glóbulos vermelhos, glóbulos brancos e plaquetas.
Essas células podem ser obtidas de três principais fontes:
1) Medula óssea – contém células-tronco adultas (ou maduras), que já estão parcialmente diferenciadas e dão origem principalmente a células do sangue e do sistema imunológico.
2) Sangue periférico – de onde podem ser isoladas células-tronco pluripotentes induzidas (iPSCs), reprogramadas em laboratório para adquirir características semelhantes às embrionárias.
3) Sangue do cordão umbilical – rico em células-tronco embrionárias, mais versáteis e menos diferenciadas, com potencial para gerar praticamente qualquer tipo celular (como neurônios, células musculares ou epiteliais).
Figura 5: Imagem obtida no freepik
Tipos e potencial de diferenciação
As células da medula óssea, por exemplo, são mais especializadas e dão origem a tecidos relacionados ao sangue e sistema imune. Já as pluripotentes (como as iPSCs) podem se transformar em mais de 200 tipos de células diferentes, abrangendo praticamente todos os tecidos do corpo. As embrionárias são as menos diferenciadas — ou seja, têm o maior potencial de transformação, podendo originar células de ossos, músculos, cérebro e pele, entre outras.
Aplicações e perspectivas
Na terapia, geralmente são utilizadas células da medula óssea e/ou do sangue periférico (como as iPSCs). O uso de células-tronco obtidas de sangue de cordão armazenado, polpa dentária ou outros tecidos ainda está em desenvolvimento.
Para garantir segurança e eficácia, é essencial investir em pesquisa básica e ampliar os estudos clínicos que validem essas novas abordagens.
Nos últimos anos, alguns estudos de destaque vêm utilizando edição gênica (como CRISPR/Cas9) para corrigir mutações em CTHs autólogas (células advindas do próprio paciente), possibilitando o tratamento de doenças hereditárias do sangue — como a anemia falciforme e a beta-talassemia (Frangoul et al., N Engl J Med, 2021).
Tipos de câncer tratados com CTHs
A terapia com células-tronco hematopoiéticas pode ser aplicada em diversos tipos de câncer e doenças hematológicas, incluindo:
- Leucemia mieloide aguda — as CTHs podem restaurar a medula após quimioterapia intensiva. (Döhner et al., Blood, 2017)*
- Leucemia linfoblástica aguda — transplantes alogênicos de CTHs têm papel essencial em casos de recaída. (Hunger & Mullighan, N Engl J Med, 2015)*
- Leucemia mieloide crônica — a TCTH continua sendo uma opção curativa em casos resistentes à terapia-alvo. (Baccarani et al., Blood, 2013)*
- Síndromes mielodisplásicas — o transplante é atualmente a única terapia potencialmente curativa. (Malcovati et al., Lancet Oncol., 2020)*
- Doenças mieloproliferativas — como policitemia vera e mielofibrose, podem ser tratadas com TCTH em estágios avançados. (Tefferi & Pardanani, Blood Cancer J., 2021)*
- Linfoma não Hodgkin — transplantes autólogos ou alogênicos melhoram a sobrevida em casos refratários. (Philip et al., N Engl J Med., 1995; Sorror et al., J Clin Oncol., 2019)*
- Linfoma de Hodgkin — a TCTH é usada quando a doença não responde a múltiplas linhas de tratamento. (Sureda et al., Blood, 2012)*
- Leucemia linfocítica crônica — indicada em casos com mutações genéticas de alto risco. (Dreger et al., Bone Marrow Transplant., 2020)*
- Mieloma múltiplo — transplante autólogo de CTHs é parte do tratamento padrão. (Attal et al., N Engl J Med., 2017)*
- Leucemia mieloide crônica juvenil — o transplante é a única opção curativa conhecida. (Locatelli et al., Blood, 2013)*
- Neuroblastoma — o transplante autólogo de CTHs é parte essencial do tratamento intensivo. (Park et al., J Clin Oncol., 2019)*
- Carcinoma renal — ainda experimental, mas com estudos avaliando seu uso em terapias combinadas.(Rini et al., Nat Rev Urol., 2020)*
- Câncer de ovário — pesquisas investigam o papel das CTHs na regeneração tecidual e resposta imune pós-quimioterapia. (Li et al., Stem Cell Res Ther., 2021)*
- Tumores de células germinativas — casos refratários podem se beneficiar do transplante autólogo. (Lorch et al., J Clin Oncol., 2012)*
A terapia celular é uma das áreas mais dinâmicas da medicina moderna. Os avanços científicos estão ampliando as possibilidades de cura e abrindo novas perspectivas para o tratamento de doenças até então sem alternativas eficazes. Apesar do potencial promissor, ainda existem desafios técnicos, regulatórios e éticos a serem superados — mas o futuro das terapias com CTHs é promissor.
Fique ligado em nosso site para mais informações!
Referências
- Frangoul H, Altshuler D, Cappellini MD, Chen YS, Domm J, Eustace BK, et al. CRISPR-Cas9 Gene Editing for Sickle Cell Disease and β-Thalassemia. N Engl J Med. 2021;384(3):252–260. doi:10.1056/NEJMoa2031054. PubMed
- Döhner H, Estey E, Grimwade D, Amadori S, Appelbaum FR, Büchner T, et al. Diagnosis and management of AML in adults: 2017 ELN recommendations from an international expert panel. Blood. 2017;129(4):424–447. doi:10.1182/blood-2016-08-733196. ASH Publications
- Hunger SP, Mullighan CG. Acute Lymphoblastic Leukemia in Children. N Engl J Med. 2015;373(16):1541–1552. doi:10.1056/NEJMra1400972. New England Journal of Medicine
- Baccarani M, Pileri S, Deininger MW, Fava C, Pane F, Cortes J, et al. Chronic myeloid leukemia: ESMO Clinical Practice Guidelines. Blood. 2013;122(6):872–884. doi:10.1182/blood-2012-12-469212. ASH Publications
- Malcovati L, Papaemmanuil E, Bowen D, Boultwood J, Della Porta MG, Pascutto C, et al. Clinical significance of SF3B1 mutations in myelodysplastic syndromes and other myeloid neoplasms. Lancet Oncol. 2020;21(8):1029–1040. doi:10.1016/S1470-2045(20)30247-7. PubMed
- Tefferi A, Pardanani A. Myeloproliferative Neoplasms: A Contemporary Review. Blood Cancer J. 2021;11(3):94. doi:10.1038/s41408-021-00476-8. ASH Publications
- Philip T, Guglielmi C, Hagenbeek A, Somers R, Van der Lelie H, Bron D, et al. Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-Hodgkin’s lymphoma. N Engl J Med. 1995;333(23):1540–1545. doi:10.1056/NEJM199512073332305. New England Journal of Medicine
- Sorror ML, Storer BE, Sandmaier BM, et al. Hematopoietic cell transplantation for non-Hodgkin lymphoma: 20-year outcomes. J Clin Oncol. 2019;37(7):566–575. doi:10.1200/JCO.18.00669. PubMed
- Sureda A, Robinson S, Canals C, et al. Reduced-intensity conditioning compared with conventional allogeneic stem-cell transplantation in relapsed or refractory Hodgkin’s lymphoma: an analysis from the Lymphoma Working Party of the EBMT. Blood. 2012;119(22):5591–5598. doi:10.1182/blood-2011-12-399725. ASH Publications
- Dreger P, Corradini P, Kimby E, et al. Indications for allogeneic stem cell transplantation in chronic lymphocytic leukemia: the EBMT consensus. Bone Marrow Transplant. 2020;55(4):611–624. doi:10.1038/s41409-019-0673-6. ASH Publications
- Attal M, Lauwers-Cances V, Hulin C, et al. Autologous transplantation for multiple myeloma in the era of new drugs: a phase III study. N Engl J Med. 2017;376(14):1311–1320. doi:10.1056/NEJMoa1611750. New England Journal of Medicine
- Locatelli F, Nöllke P, Zecca M, et al. Hematopoietic stem cell transplantation in children with juvenile myelomonocytic leukemia: results of the EWOG-MDS study. Blood. 2013;121(25):5058–5066. doi:10.1182/blood-2013-02-482570. ASH Publications
- Park JR, Kreissman SG, London WB, et al. Effect of Tandem Autologous Stem Cell Transplant vs Single Transplant on Event-Free Survival in High-Risk Neuroblastoma: A Randomized Clinical Trial. J Clin Oncol. 2019;37(25):2056–2065. doi:10.1200/JCO.19.00467. PubMed
- Rini BI, Campbell SC, Escudier B. Renal cell carcinoma. Nat Rev Urol. 2020;17(5):313–325. doi:10.1038/s41585-020-0329-9. ASH Publications
- Li Y, Feng Y, Wang X, et al. Mesenchymal stem cells in ovarian cancer: a double-edged sword. Stem Cell Res Ther. 2021;12(1):1–12. doi:10.1186/s13287-021-02410-8. ASH Publications
- Lorch A, Bascoul-Mollevi C, Kramar A, et al. Conventional-dose versus high-dose chemotherapy as first salvage treatment in male patients with metastatic germ cell tumors: evidence from a large international database. J Clin Oncol. 2012;30(8):870–876. doi:10.1200/JCO.2011.38.0637. PubMed
- https://www.uchicagomedicine.org/cancer/types-treatments/cellular-therapy
- https://br.freepik.com/fotos-gratis/medico-e-paciente-de-maos-dadas-apos-close-up-de-mas-noticias_11191133.htm#from_view=detail_alsolike
- https://br.freepik.com/fotos-gratis/formacao-medica-3d-com-celulas-de-virus-e-fita-de-dna_2795501.htm#fromView=search&page=1&position=2&uuid=1ff471a8-79e1-479a-97b4-50c447087925
- https://bvsms.saude.gov.br/imunoterapia-contra-celulas-do-cancer-custo-acesso-e-efetividade/
